







(ДВС-синдром)-нарушение гемостаза, в основе которого лежит распространенное свертывание крови с образованием большого количества микросгустков и агрегатов клеток крови, что приводит к нарушению микроциркуляции в органах и тканях, развитию выраженных дистрофических изменений.
Этиология. ДВС-синдром развивается при различных ситуациях — хирургических вмешательствах, акушерской патологии, сепсисе, злокачественных опухолях, а также при некоторых терапевтических заболеваниях и состояниях — гемобластозах, острой и хронической почечной недостаточности, системных васкулитах, остром гемолизе.Патогенез. Изменение состояния свертывающей и противосвертывающей систем при развитии ДВС-синдрома проходит несколько стадий.В начальной стадии (стадия гиперкоагуляции) под влиянием различных экзогенных (продукты жизнедеятельности бактерий, змеиные яды, трансфузионные средства и пр.) и эндогенных (продукты протеолиза и цитолиза, тканевый тромбопластин и др.) факторов активируются процессы свертывания крови и агрегации тромбоцитов.Затем происходит выпадение тромбов, чему способствует также попадание в кровоток большого количества продуктов белкового распада под влиянием одновременной активации других систем — фибринолитической, калликреин-кининовой. Множественное тромбообразование приводит к нарушению микроциркуляции и изменениям функций различных органов и систем.
Активация свертывания крови вызывает истощение противосвертывающих механизмов-
физиологических антикоагулянтов (системы «гепарин — антитромбин III») и фибринолитической системы «плазминоген-плазмин». Множественное тромбообразование влечет за собой так назы-ваемую коагулопатию потребления (снижение содержания плазменных факторов свертывания) и тромбоцитопению, что обусловливает развитие геморрагического синдрома.
Принято различать острый ДВС-синдром (развитие идет в пределах су¬ток), подострый (развивается в течение нескольких суток — недели), хро¬нический (протекает многие недели и месяцы). В течении ДВС-синдрома условно выделяют четыре стадии: 1) гиперкоагуляция и агрегация; 2) переходная с нарастающей коагуляцией, тромбоцитопенией и разнонаправленными сдвигами в различных коагуляционных тестах; 3) гипокоагуляция; 4) восстановительная.
Лечение. Лечение ДВС-синдрома должно включать мероприятия, направленные на устранение причины его развития (лечение инфекционных процессов, основного заболевания), борьбу с шоком, коррекцию гемостаза.•Трансфузии свежезамороженной плазмы — один из основных мето¬дов лечения острого ДВС-синдрома (гепарин добавляют для того, чтобы плазма не свернулась). Свежезамороженная плазма содержит антитромбин III, плазминоген, факторы свертывания и естественные антиагреганты. •Массивные трансфузии свежезамороженной плазмы осуществляют под прикрытием профилактических доз гепарина по 2500—5000 ЕД 2 раза в сутки подкожно. В настоящее время используют также низкомолекулярный гепарин — фраксипарин по 0,3—0,5 мл подкожно или клексан по 40 мг/сут подкожно. При резкой активации фибринолиза необходимо введение 100 000 ЕД/сут контрикала или других антипротеаз в максимальных Дозах. При профузных маточных, носовых, желудочно-кишечных, легоч¬ных кровотечениях внутривенно вводят тромбоконцентраты. Локальная остановка кровотечений — тампонады, перекись водорода, ПАМБА, ами-нокапроновая кислота, дицинон (этамзилат) в виде аппликаций, турунд, смоченных раствором дицинона (в нос), внутрь и парентерально.В настоящее время используют супернатантную плазму, имеющую меньшую тенденцию к свертыванию, чем свежезамороженная плазма, в ней содержится меньше фибриногена, фактора VIII, фибронектина и фак¬тора Виллебранда. Таким образом, появилась возможность замещения ес¬тественных физиологических антикоагулянтов при массивных тромбозах.
• Плазмаферез и плазмозамену, позволяющие удалять активность свертывания и продукты паракоагуляции, широко используют при иммунокомплексном синдроме, тканевом распаде, некрозе, выраженном геморрагиче¬ском синдроме, септическом шоке, ожогах, при синдроме раздавливания тканей, улучшают гемодинамику, предупреждают развитие острой почеч¬ной недостаточности.
• При выявлении бактериемии (в большинстве случаев острого ДВС-синдрома) необходимо назначать антибиотики (не очень токсичные) для стерилизации кишечника.
• Трансфузии эритроцитной массы осуществляют в редких случаях — лишь при острой кровопотере (более 1 л крови), так как в крови донора содержится много активаторов свертывания крови.
• Для защиты эндотелия от бактериальных эндотоксинов используют эндотелиопротекторы (интерлейкины, цитокины, факторы некроза опухо¬лей, медиаторы воспаления).
studfiles.net
(ДВС-синдром)-нарушение гемостаза, в основе которого лежит распространенное свертывание крови с образованием большого количества микросгустков и агрегатов клеток крови, что приводит к нарушению микроциркуляции в органах и тканях, развитию выраженных дистрофических изменений.
Этиология. ДВС-синдром развивается при различных ситуациях — хирургических вмешательствах, акушерской патологии, сепсисе, злокачественных опухолях, а также при некоторых терапевтических заболеваниях и состояниях — гемобластозах, острой и хронической почечной недостаточности, системных васкулитах, остром гемолизе.Патогенез. Изменение состояния свертывающей и противосвертывающей систем при развитии ДВС-синдрома проходит несколько стадий.В начальной стадии (стадия гиперкоагуляции) под влиянием различных экзогенных (продукты жизнедеятельности бактерий, змеиные яды, трансфузионные средства и пр.) и эндогенных (продукты протеолиза и цитолиза, тканевый тромбопластин и др.) факторов активируются процессы свертывания крови и агрегации тромбоцитов.Затем происходит выпадение тромбов, чему способствует также попадание в кровоток большого количества продуктов белкового распада под влиянием одновременной активации других систем — фибринолитической, калликреин-кининовой. Множественное тромбообразование приводит к нарушению микроциркуляции и изменениям функций различных органов и систем.
Активация свертывания крови вызывает истощение противосвертывающих механизмов-
физиологических антикоагулянтов (системы «гепарин — антитромбин III») и фибринолитической системы «плазминоген-плазмин». Множественное тромбообразование влечет за собой так назы-ваемую коагулопатию потребления (снижение содержания плазменных факторов свертывания) и тромбоцитопению, что обусловливает развитие геморрагического синдрома.
Принято различать острый ДВС-синдром (развитие идет в пределах су¬ток), подострый (развивается в течение нескольких суток — недели), хро¬нический (протекает многие недели и месяцы). В течении ДВС-синдрома условно выделяют четыре стадии: 1) гиперкоагуляция и агрегация; 2) переходная с нарастающей коагуляцией, тромбоцитопенией и разнонаправленными сдвигами в различных коагуляционных тестах; 3) гипокоагуляция; 4) восстановительная.
Лечение. Лечение ДВС-синдрома должно включать мероприятия, направленные на устранение причины его развития (лечение инфекционных процессов, основного заболевания), борьбу с шоком, коррекцию гемостаза.•Трансфузии свежезамороженной плазмы — один из основных мето¬дов лечения острого ДВС-синдрома (гепарин добавляют для того, чтобы плазма не свернулась). Свежезамороженная плазма содержит антитромбин III, плазминоген, факторы свертывания и естественные антиагреганты. •Массивные трансфузии свежезамороженной плазмы осуществляют под прикрытием профилактических доз гепарина по 2500—5000 ЕД 2 раза в сутки подкожно. В настоящее время используют также низкомолекулярный гепарин — фраксипарин по 0,3—0,5 мл подкожно или клексан по 40 мг/сут подкожно. При резкой активации фибринолиза необходимо введение 100 000 ЕД/сут контрикала или других антипротеаз в максимальных Дозах. При профузных маточных, носовых, желудочно-кишечных, легоч¬ных кровотечениях внутривенно вводят тромбоконцентраты. Локальная остановка кровотечений — тампонады, перекись водорода, ПАМБА, ами-нокапроновая кислота, дицинон (этамзилат) в виде аппликаций, турунд, смоченных раствором дицинона (в нос), внутрь и парентерально.В настоящее время используют супернатантную плазму, имеющую меньшую тенденцию к свертыванию, чем свежезамороженная плазма, в ней содержится меньше фибриногена, фактора VIII, фибронектина и фак¬тора Виллебранда. Таким образом, появилась возможность замещения ес¬тественных физиологических антикоагулянтов при массивных тромбозах.
• Плазмаферез и плазмозамену, позволяющие удалять активность свертывания и продукты паракоагуляции, широко используют при иммунокомплексном синдроме, тканевом распаде, некрозе, выраженном геморрагиче¬ском синдроме, септическом шоке, ожогах, при синдроме раздавливания тканей, улучшают гемодинамику, предупреждают развитие острой почеч¬ной недостаточности.
• При выявлении бактериемии (в большинстве случаев острого ДВС-синдрома) необходимо назначать антибиотики (не очень токсичные) для стерилизации кишечника.
• Трансфузии эритроцитной массы осуществляют в редких случаях — лишь при острой кровопотере (более 1 л крови), так как в крови донора содержится много активаторов свертывания крови.
• Для защиты эндотелия от бактериальных эндотоксинов используют эндотелиопротекторы (интерлейкины, цитокины, факторы некроза опухо¬лей, медиаторы воспаления).
studfiles.net
ДВС-синдром возникает обычно в результате поступления в кровь или образования в ней веществ, инициирующих свертывание крови. Основополагающее событие в генезе острого ДВС-синдрома -
чрезмерная активация свертывающей системы крови с образованием избытка тромбина, сопровождающаяся падением уровня тромбоцитов и факторов свертывания крови. К этому синдрому чаще всего могут приводить следующие состояния:
1.
Повреждение тканей (массивный контакт крови с тканевым фактором):
• Механическая травма (краш-синдром,проникающие повреждения, напримерповреждения мозга).
• Термальные повреждения (ожоги, обморожения).
• Асфиксия и гипоксия.
• Оперативные вмешательства.
• Ишемия органов, инфаркты.
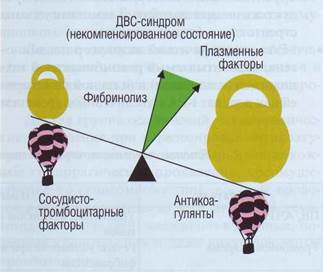
Рис. 144. ДВС-синдром - состояние, при котором развивается декомпенсация, динамическое равновесие не достигается из-за чрезмерной активации факторов, вызывающих гиперкоагуляцию
Патология гемостаза
• Жировая эмболия.
• Гиповолемический/геморрагический/анафилактический шок.
• Гипертермия.
2. Онкология (контакт с онкологическими про-коагулянтами, тканевым фактором, факторомнекроза опухоли, клеточными протеазами):
• Солидные опухоли.
• Лейкозы.
3. Инфекция (воздействие эндотоксинов, повреждение эндотелиальных клеток, активация тромбоцитов):
• Бактериальные инфекции, вызванные менингококками, Е. coli, Salmonella, Pseudo-monas, Haemophilus, Pneumococcus,Hemolytic streptococci, Staphylococcus.
• Вирусные инфекции, вызванные Dengue,Lassa, Ebola, Marburg, Hantaan, Rubella,Herpes и др.
• Протозойные - малярия.
• Другие - кандидозы, аспаргиллезы, кло-стридиозы, туберкулез.
• Токсический шок.
• Грамотрицательный сепсис.
4. Патология сосудов и циркуляторные нарушения(поражение эндотелия, активация тромбоцитов):
• Гигантская гемангиома, сосудистые опухоли.
• Аневризма аорты.
• Хирургические вмешательства на сосудах, внутрисосудистые манипуляции.
• Опухоли сердца.
• Операции шунтирования сосудов сердца.
• Острый инфаркт миокарда.
• Васкулиты.
• Эмболия легочной артерии.
5. Иммунологические нарушения (активациякомплемента, экспозиция тканевого фактора):
• Анафилактические реакции.
• Аллергические реакции.
• Острые гемолитические посттрансфузи-онные реакции.
• Гепарин-индуцированная тромбоцито-пения.
• Реакция отторжения трансплантата.
• Болезнь Кавасаки.
6. Прямая активация ферментов:
• Панкреатит.
• Укусы ядовитых змей.
7. Другие расстройства:
• Фульминантный некроз печени.
• Синдром Рейе.
• Цирроз печени.
• Респираторный дистресс-синдром увзрослых.
• Инфузия концентратов протромбиново-го комплекса.
• Гемолитико-уремический синдром.
• Воспалительные заболевания кишечника,перитонит.
• Саркоидоз, амилоидоз.
• Геморрагический шок.
• Гомозиготный дефицит протеинов С и S.
8. Осложнения беременности:
• Преждевременная отслойка плаценты.
• Эмболия амниотическими водами.
• Эклампсия и преэклампсия.
• Индуцированные аборты.
• Внутриутробная гибель плода или незаконченный аборт.
• Сросшаяся плацента.
• Разрыв матки.
• Хроническая трубная беременность.
• Дегенеративная фибромиома.
• Внутриутробная гибель одного из однояйцевых близнецов.
9. ДВС у новорожденных:
• Инфекции.
• Асфиксия в родах.
• Болезнь гиалиновых мембран.
• Аспирационный синдром, апноэ, ателектаз, пневмония.
• Легочное кровотечение.
• Переохлаждение.
• Глубокая недоношенность.
• Тромбозы крупных сосудов.
• Фульминантная пурпура.
• Некротизирующий энтероколит.
• Новообразования у плода и лейкозы.
• Повреждение головного мозга (некрозыи кровоизлияния).
• Фетальный эритробластоз.
• Поражение печени.
• Врожденное нарушение толерантности кфруктозе.
Основные патогенетические механизмы запуска ДВС:
• Нарушение или повреждение эндотелия, сопровождающееся высвобождением прокоагу-
Патология гемостаза
лянтов и контактом крови с тканевым фактором.
• Активация моноцитов с экспрессией тканевого фактора и прокоагулянтов моноцитов.Именно чрезмерная активация и дегрануля-ция моноцитов-макрофагов, обладающихполноценным кровяным тромбопластином,часто рассматривается как центральное звено ДВС-синдрома при сепсисе.
• Контакт с тканевым фактором клеток злокачественных опухолей. ДВС особенно часто возникает при аденокарциноме поджелудочной и предстательной желез, продуцирующей муцин, при остром промиелоцитар-ном лейкозе, при котором гипергранулярные лейкозные клетки высвобождают изгранул материал, подобный тканевому фактору.
• Массивное поступление в кровь физиологических прокоагулянтов при различных повреждениях, массивных травмах, эмболии идр. Травмы головы с нарушением гематоэн-цефалического барьера и контактом крови стканью мозга - мощный источник тканевоготромбопластина. Осложнения беременности,при которых материал, обладающий активностью тканевого фактора, попадает из полости матки в кровь матери (преждевременная отслойка плаценты, аборт, задержка мертворожденного плода или эмболия околоплодной жидкостью).
• Шок с выпадением функции органов и развитием полиорганной недостаточности.
• Введение факторов протромбинового комплекса, особенно активированных (переливание несовместимой крови).
• Массивное поступление в кровь бактериальных прокоагулянтов. В капсиде бактерийприсутствует большое количество липополи-сахаридов (эндотоксин, рис. 145), способныхрезко активировать моноциты-макрофагисистемы циркуляции.
• Прямая активация ферментами змеиныхядов.
Ведущую роль в запуске патологических процессов при ДВС, как правило, играет внешний путь активации протромбина. Активизация контактных факторов при ДВС-синдроме в первую очередь приводит к гипотонии и вазодилатации.

Рис. 145. Эндотоксинкапсида бактерий. Особенно его много у грамотрицательных бактерий. Эндотоксин вызывает массивную активацию с дегрануляцией моноцитов-макрофагов и освобождение в кровь большого количества кровяного тромбопластина, который индуцирует гиперкоагуляцию и развитие ДВС-синдрома
Еще одним звеном развития патологического свертывания крови и особенно синдрома потребления является повреждение тромбоцитов и эритроцитов. Кислые фосфолипиды, в норме находящиеся на внутренней поверхности клеточной мембраны, являются важным фактором активации процессов свертывания крови. Их появление в циркулирующей крови в большом количестве приводит к значительному усилению процесса свертывания крови и потреблению прокоагулянтов. Возможно, что активация системы комплемента также усиливает процесс потребления, но более вероятно, что это лишь два параллельных процесса.
Имеются данные, что у пациентов с коагуло-патией потребления снижена функция тканевых макрофагов и содержание фибронектина. Это приводит к снижению активности удаления макрофагами ретикулоэндотелиальной системы микроагрегатов фибрина, обломков коллагена и, возможно, бактерий и продуктов их жизнедеятельности.
Виды ДВС-синдрома
Лабораторные показатели, характеризующие состояние гиперкоагуляции и внутрисосудисто-го свертывания, меняются в зависимости от тече-
Патология гемостаза
ния и стадии процесса. По течению ДВС-синдром подразделяют на:
• Острый, включая молниеносную (катастрофическую) форму. Острый ДВС-синдром проявляется комплексом аномалий, включающим нарушение микроциркуляции, повреждение сосудистой стенки, тромбоцитопениюи тромбоцитопатию, анизоцитоз и гемолизэритроцитов, нейтрофильную реакцию, гиперкоагуляцию и геморрагический синдромна фоне коагулопатии и тромбоцитопатиипотребления, нарушения в системах фибри-нолиза, антикоагулянтов, калликреин-кини-новой и других протеолитических систем.Фазы острого ДВС-синдрома:
1) гиперкоагуляция и гиперагрегация;
2) коагулопатия и тромбоцитопатия потребления с активацией фибринолитичес-кой системы;
3) генерализация фибринолиза;
4) восстановление.
• Подострый с длительным периодом гиперкоагуляции и/или гиперагрегации тромбоцитов.Подострый ДВС-синдром, характеризующийся вялотекущим, скорее хроническим течением, лабораторно проявляется тромбоци-топенией, нормальным или несколько удлиненным ПВ, укорочением АЧТВ, нормальным или несколько сниженным фибриногеном и повышением уровня в плазме продуктов деградации фибрина (ПДФ). Следует отметить, что фибриноген, как острофазныйбелок, при инфекционных и травматическихформах ДВС может быть повышенным. Этосостояние может приводить к тромбоэмболи-ческим осложнениям, в том числе к тромбозам вен, артериальной тромбоэмболии. Кровоточивость встречается нечасто.
• Хронический. Для хронической формы ДВС-синдрома характерно постоянное, но менеесильное активирующее воздействие на систему гемостаза. Это обуславливает малую скорость генерации тромбина, однако достаточную для развития микроциркуляторных нарушений. Хроническая форма ДВС-синдрома наблюдается при хронических заболеваниях легких, почек, атеросклерозе, сахарномдиабете, артериальной гипертензии и другихзаболеваниях.
poznayka.org
Независимо от того, по какому механизму произошло образование тромбина (в силу активации внутреннего или внешнего пути), с этого момента развиваются сложные цепи причинно-следственных изменений как в системе гемостаза, так и в других системах организма.
Основная опасность для организма, возникающая в результате ДВС - распространенные расстройства микроциркуляции, приводящие к дистрофии, некрозам и глубокому нарушению функции различных органов.
Расстройство микроциркуляции при ДВС имеет ряд механизмов:
Основным является образование в просвете сосудов сгу стков фибрина и агрегатов из тромбоцитов и эритроцитов. Сгу стки фибрина появляются в крови не сразу. В начале молекулы фибрин-мономера образуют с фибриногеном растворимые комплексы (растворимый фибрин). Однако по мере того, как уменьшается количество фибриногена, фибрин становится не растворимым. Нерастворимым его делает и активируемый тромбином ХШ фактор. Сгустки фибрина и агрегаты клеток ("сладж—феномен") вызывают распространенную эмболию капилляров.
Под влиянием фактора ХПа и тромбина активируются не сколько взаимосвязанных протеолитических систем плазмы: фибринолитическая, калликреиновая и система комплемента. Поэтому об остром ДВС говорят как о "гуморальном проте- азном взрыве". Последствия его очень разнообразны. В част ности, активированные протеолитические ферменты повреж дают стенки капилляров, что в свою очередь способствует даль нейшей активации свертывающей системы крови, а кроме того вызывает распространенное тромбообразование.
3. В результате ДВС ухудшаются реологические свойства крови - ее текучесть. Это связано со "сладж-феноменом", а
83
также со сгущением крови в капиллярах в результате снижения их гемодилюционной способности из-за повреждения про-теазами, а также повышения проницаемости под влиянием ки-нинов и гистамина. Кинины образуются в результате активации фактором Хагемана калликреиновой системы. Гистамин выделяется из тучных клеток сосудов в комплексе с гепарином, фактором противосвертывающей системы. Гепарин расходуется в процессе взаимодействия с факторами коагуляции и резервы его истощаются, а уровень гистамина растет. Кроме того, гистамин поступает из тканей в результате их гипоксии и некроза.
Микроциркуляция страдает из-за разнонаправленных из менений тонуса сосудов. Кинины, гистамин снижают его, а серотонин и тромбоксан А2, выделяющиеся при агрегации тром боцитов, вызывают спазм. Способность сосудов противосто ять спазмирующему влиянию тромбоксана путем выработки простациклина снижена в результате их повреждения. В ре зультате нарушений тонуса сосудов и снижения реологических свойств крови (в связи со сгущением, образованием сгустков фибрина, агрегатов клеток, набуханием эритроцитов) крово ток по капиллярам резко замедляется, вплоть до стаза.
Стазы, эмболы, тромбы приводят не только к местным нарушениям, но и к системному расстройству кровообращения. Вследствие нарушенной проходимости сосудов печени кровь скапливается в портальной системе и уменьшается приток к правому сердцу. Эмболия легочных капилляров, спазм и тром боз сосудов малого круга препятствуют притоку к левому сер дцу. В результате уменьшения сердечного выброса может чрезвычайно резко снизиться артериальное давление в боль шом круге, что усугубляет расстройство микроциркуляции.
6. По мере развития ДВС может возникать дефицит фак торов противосвертывающей системы (антитромбин III) и фибри- нолитической (плазминоген и его активаторы - прекалликреино- ген и высокомолекулярный кининоген). Это способствует обра зованию тромбов и препятствует лизису сгустков в кровотоке.
studfiles.net
 Патогенез ДВС синдрома
Патогенез ДВС синдрома
 Каждый человек встречается с ДВС синдромом как минимум дважды: когда рождается и когда умирает. А. И. Воробьев Нитью фибрина начинается и заканчивается жизнь человека.
Каждый человек встречается с ДВС синдромом как минимум дважды: когда рождается и когда умирает. А. И. Воробьев Нитью фибрина начинается и заканчивается жизнь человека.
 ДВС синдром - синдром полиорганной недостаточности , в основе которого лежит внутрисосудистая активация коагуляции , ведущая к блокаде микроциркуляции рыхлыми массами фибрина и агрегатами клеток, с потреблением про- и антикоагулянтов, что может сопровождается клиникой тромбозов и геморрагий. Н. П. Шабалов
ДВС синдром - синдром полиорганной недостаточности , в основе которого лежит внутрисосудистая активация коагуляции , ведущая к блокаде микроциркуляции рыхлыми массами фибрина и агрегатами клеток, с потреблением про- и антикоагулянтов, что может сопровождается клиникой тромбозов и геморрагий. Н. П. Шабалов
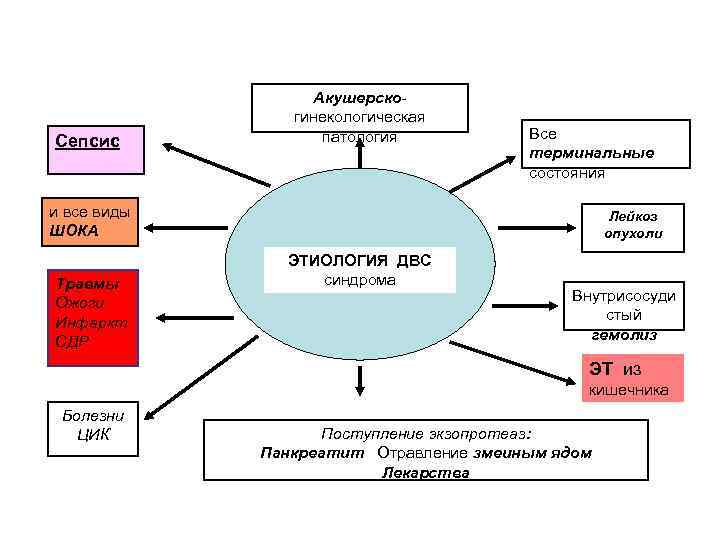 Акушерско- гинекологическая Сепсис патология Все терминальные состояния и все виды Лейкоз ШОКА опухоли ЭТИОЛОГИЯ ДВС Травмы синдрома Ожоги Внутрисосуди Инфаркт стый СДР гемолиз ЭТ из кишечника Болезни ЦИК Поступление экзопротеаз: Панкреатит Отравление змеиным ядом Лекарства
Акушерско- гинекологическая Сепсис патология Все терминальные состояния и все виды Лейкоз ШОКА опухоли ЭТИОЛОГИЯ ДВС Травмы синдрома Ожоги Внутрисосуди Инфаркт стый СДР гемолиз ЭТ из кишечника Болезни ЦИК Поступление экзопротеаз: Панкреатит Отравление змеиным ядом Лекарства
 8. 4% 12. 7% 66. 2%
8. 4% 12. 7% 66. 2%
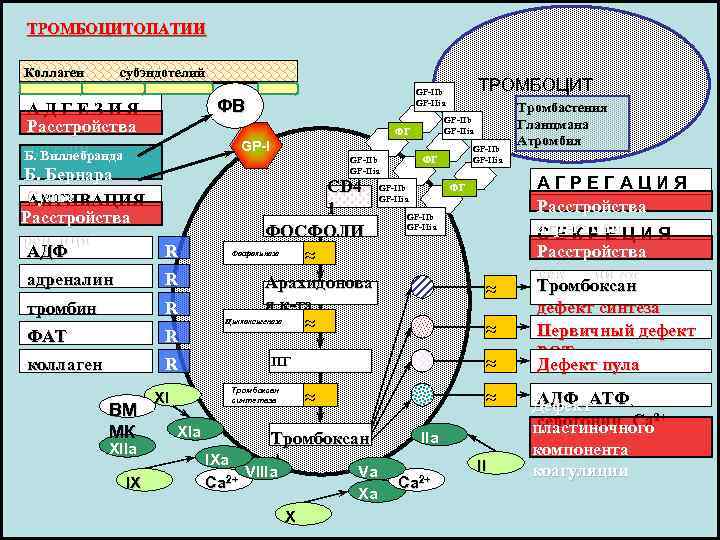 ТРОМБОЦИТОПАТИИ Коллаген субэндотелий GP-IIb ТРОМБОЦИТ А Д Г Е З И Я ФВ GP-IIia Тромбастения GP-IIb Расстройства ФГ GP-IIia Гланцмана Атромбия адгезии Б. Виллебранда GP-IIb GP-IIb ФГ GP-IIia Б. Бернара GP-IIia А Г Р Е Г А Ц И Я CD 4 GP-IIb ФГ Сулье АКТИВАЦИЯ GP-IIia 1 Расстройства GP-IIb ФОСФОЛИ GP-IIia агрегации С Е К Р Е Ц И Я рецепции АДФ R ПИДЫ Фосфолипаза Расстройства адреналин R секреции РОТ Арахидонова Тромбоксан тромбин R я к-та дефект синтеза Циклоксигеназа тромбоксана Первичный дефект ФАТ R РОТ коллаген R ПГ Дефект пула хранения XI Тромбоксан синтетаза АДФ¸ АТФ¸ ВМ Дефект серотонин¸ Са 2+ пластиночного МК XIa Тромбоксан IIa XIIa компонента IXa А 2 II VIIIa Va коагуляции IX Ca 2+ Xa X
ТРОМБОЦИТОПАТИИ Коллаген субэндотелий GP-IIb ТРОМБОЦИТ А Д Г Е З И Я ФВ GP-IIia Тромбастения GP-IIb Расстройства ФГ GP-IIia Гланцмана Атромбия адгезии Б. Виллебранда GP-IIb GP-IIb ФГ GP-IIia Б. Бернара GP-IIia А Г Р Е Г А Ц И Я CD 4 GP-IIb ФГ Сулье АКТИВАЦИЯ GP-IIia 1 Расстройства GP-IIb ФОСФОЛИ GP-IIia агрегации С Е К Р Е Ц И Я рецепции АДФ R ПИДЫ Фосфолипаза Расстройства адреналин R секреции РОТ Арахидонова Тромбоксан тромбин R я к-та дефект синтеза Циклоксигеназа тромбоксана Первичный дефект ФАТ R РОТ коллаген R ПГ Дефект пула хранения XI Тромбоксан синтетаза АДФ¸ АТФ¸ ВМ Дефект серотонин¸ Са 2+ пластиночного МК XIa Тромбоксан IIa XIIa компонента IXa А 2 II VIIIa Va коагуляции IX Ca 2+ Xa X
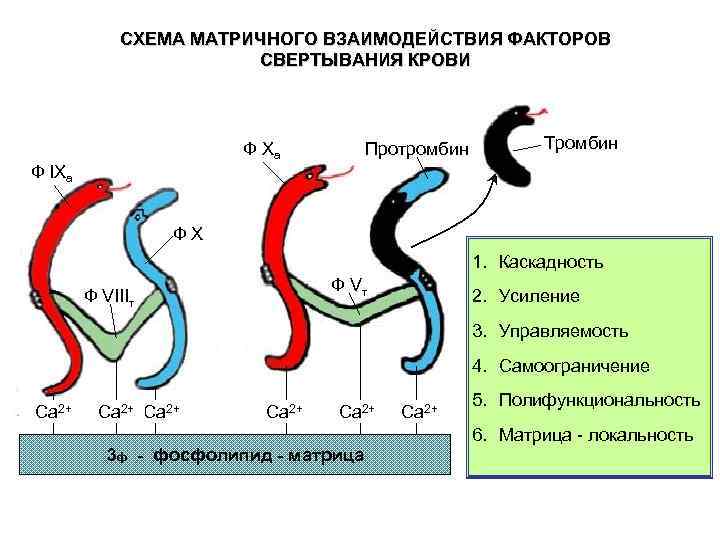 СХЕМА МАТРИЧНОГО ВЗАИМОДЕЙСТВИЯ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ Ф Xa Протромбин Тромбин Ф IXa ФX 1. Каскадность Ф Vт Ф VIIIт 2. Усиление 3. Управляемость 4. Самоограничение 5. Полифункциональность Ca 2+ Ca 2+ 6. Матрица - локальность 3 ф - фосфолипид - матрица
СХЕМА МАТРИЧНОГО ВЗАИМОДЕЙСТВИЯ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ Ф Xa Протромбин Тромбин Ф IXa ФX 1. Каскадность Ф Vт Ф VIIIт 2. Усиление 3. Управляемость 4. Самоограничение 5. Полифункциональность Ca 2+ Ca 2+ 6. Матрица - локальность 3 ф - фосфолипид - матрица
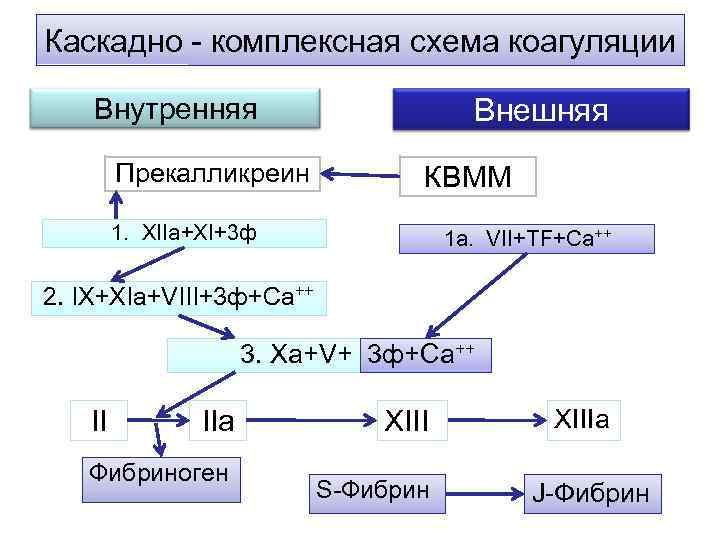 Каскадно - комплексная схема коагуляции Внутренняя Внешняя Прекалликреин КВММ 1. XIIa+XI+3 ф 1 а. VII+TF+Ca++ 2. IX+XIa+VIII+3 ф+Ca++ 3. Xa+V+ 3 ф+Са++ II IIa XIIIa Фибриноген S-Фибрин J-Фибрин
Каскадно - комплексная схема коагуляции Внутренняя Внешняя Прекалликреин КВММ 1. XIIa+XI+3 ф 1 а. VII+TF+Ca++ 2. IX+XIa+VIII+3 ф+Ca++ 3. Xa+V+ 3 ф+Са++ II IIa XIIIa Фибриноген S-Фибрин J-Фибрин
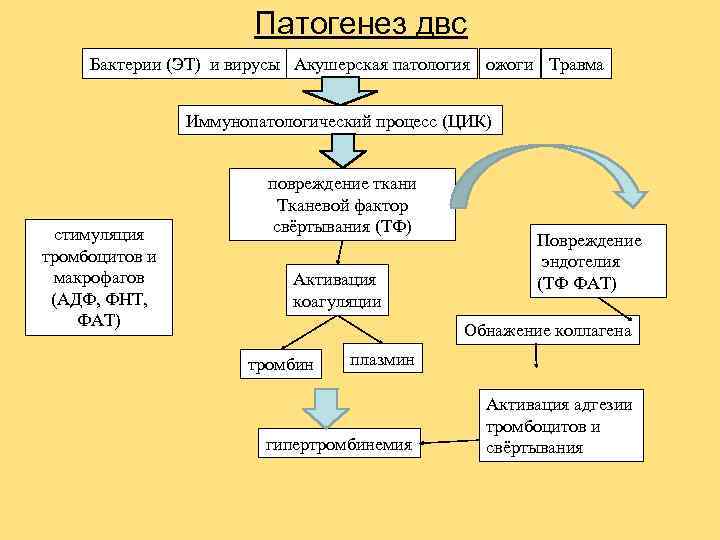 Патогенез двс Бактерии (ЭТ) и вирусы Акушерская патология ожоги Травма Иммунопатологический процесс (ЦИК) повреждение ткани Тканевой фактор стимуляция свёртывания (ТФ) Повреждение тромбоцитов и эндотелия макрофагов Активация (ТФ ФАТ) (АДФ, ФНТ, коагуляции ФАТ) Обнажение коллагена тромбин плазмин Активация адгезии тромбоцитов и гипертромбинемия свёртывания
Патогенез двс Бактерии (ЭТ) и вирусы Акушерская патология ожоги Травма Иммунопатологический процесс (ЦИК) повреждение ткани Тканевой фактор стимуляция свёртывания (ТФ) Повреждение тромбоцитов и эндотелия макрофагов Активация (ТФ ФАТ) (АДФ, ФНТ, коагуляции ФАТ) Обнажение коллагена тромбин плазмин Активация адгезии тромбоцитов и гипертромбинемия свёртывания
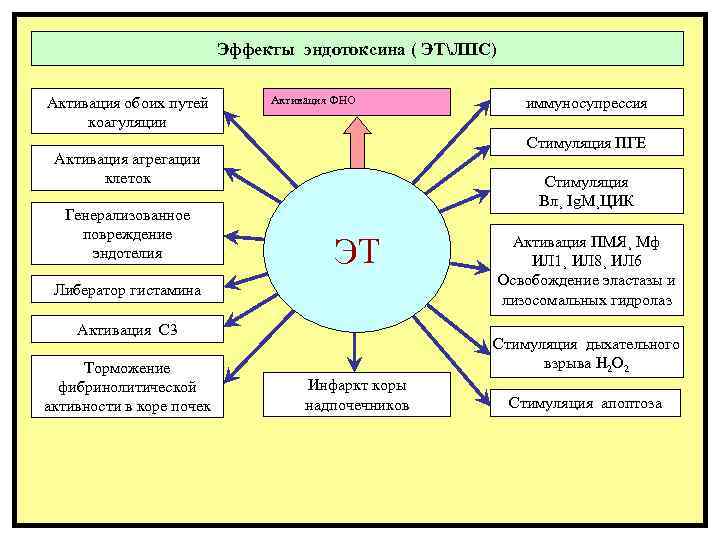 Эффекты эндотоксина ( ЭТЛПС) Активация обоих путей Активация ФНО иммуносупрессия коагуляции Стимуляция ПГЕ Активация агрегации клеток Стимуляция Вл¸ Ig. M¸ЦИК Генерализованное повреждение эндотелия ЭТ Активация ПМЯ¸ Мф ИЛ 1¸ ИЛ 8¸ ИЛ 6 Освобождение эластазы и Либератор гистамина лизосомальных гидролаз Активация С 3 Терапия: зависит от ВИДА шока и Hardway стадии Стимуляция дыхательного Торможение 1 обратимый взрыва Н 2 О 2 анальгетики¸ восполнение объема или крови¸ (ранний¸ оздний¸ допамин¸ О 2 ¸ сода¸ глюкокортикоиды¸ фибринолитической устойчивый) Инфаркт коры антиаритмические¸ электролиты¸ глюкоза¸ активности в коре почек 2. Необратимый надпочечников инсулин¸ гепарин ¸ диуретики¸ Стимуляция апоптоза кокарбоксилаза ИВЛ¸ АИК
Эффекты эндотоксина ( ЭТЛПС) Активация обоих путей Активация ФНО иммуносупрессия коагуляции Стимуляция ПГЕ Активация агрегации клеток Стимуляция Вл¸ Ig. M¸ЦИК Генерализованное повреждение эндотелия ЭТ Активация ПМЯ¸ Мф ИЛ 1¸ ИЛ 8¸ ИЛ 6 Освобождение эластазы и Либератор гистамина лизосомальных гидролаз Активация С 3 Терапия: зависит от ВИДА шока и Hardway стадии Стимуляция дыхательного Торможение 1 обратимый взрыва Н 2 О 2 анальгетики¸ восполнение объема или крови¸ (ранний¸ оздний¸ допамин¸ О 2 ¸ сода¸ глюкокортикоиды¸ фибринолитической устойчивый) Инфаркт коры антиаритмические¸ электролиты¸ глюкоза¸ активности в коре почек 2. Необратимый надпочечников инсулин¸ гепарин ¸ диуретики¸ Стимуляция апоптоза кокарбоксилаза ИВЛ¸ АИК
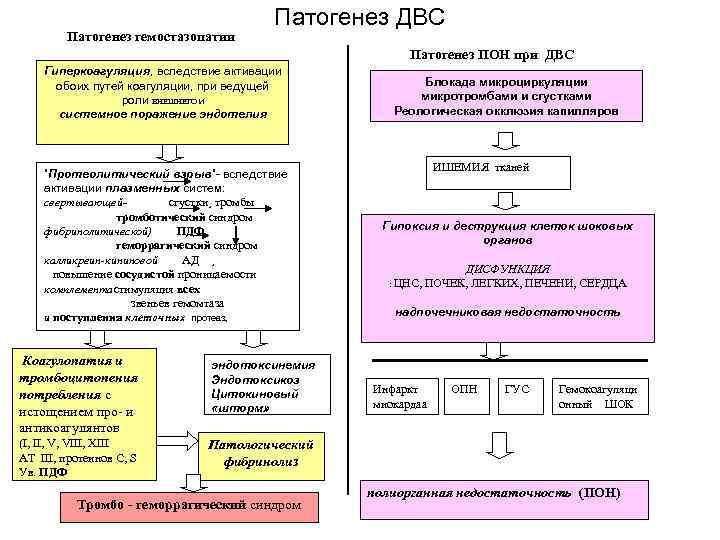 Патогенез ДВС Патогенез гемостазопатии Патогенез ПОН при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей Блокада микроциркуляции роли ВНЕШНЕГО и микротромбами и сгустками системное поражение эндотелия Реологическая окклюзия капилляров ИШЕМИЯ тканей ”Протеолитический взрыв”- вследствие активации плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ Гипоксия и деструкция клеток шоковых геморрагический синдром органов калликреин-кининовой АД ¸ повышение сосудистой проницаемости ДИСФУНКЦИЯ : ЦНС, ПОЧЕК, ЛЕГКИХ, ПЕЧЕНИ, СЕРДЦА комплементастимуляция всех звеньев гемомтаза и поступления клеточных протеаз надпочечниковая недостаточность Коагулопатия и эндотоксинемия тромбоцитопения Эндотоксикоз потребления с Цитокиновый Инфаркт ОПН ГУС Гемокоагуляци «шторм» миокардаа онный ШОК истощением про- и антикоагулянтов (I II V VIII XIII Патологический АТ III протеинов C S фибринолиз Ув. ПДФ полиорганная недостаточность (ПОН) Тромбо - геморрагический синдром
Патогенез ДВС Патогенез гемостазопатии Патогенез ПОН при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей Блокада микроциркуляции роли ВНЕШНЕГО и микротромбами и сгустками системное поражение эндотелия Реологическая окклюзия капилляров ИШЕМИЯ тканей ”Протеолитический взрыв”- вследствие активации плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ Гипоксия и деструкция клеток шоковых геморрагический синдром органов калликреин-кининовой АД ¸ повышение сосудистой проницаемости ДИСФУНКЦИЯ : ЦНС, ПОЧЕК, ЛЕГКИХ, ПЕЧЕНИ, СЕРДЦА комплементастимуляция всех звеньев гемомтаза и поступления клеточных протеаз надпочечниковая недостаточность Коагулопатия и эндотоксинемия тромбоцитопения Эндотоксикоз потребления с Цитокиновый Инфаркт ОПН ГУС Гемокоагуляци «шторм» миокардаа онный ШОК истощением про- и антикоагулянтов (I II V VIII XIII Патологический АТ III протеинов C S фибринолиз Ув. ПДФ полиорганная недостаточность (ПОН) Тромбо - геморрагический синдром
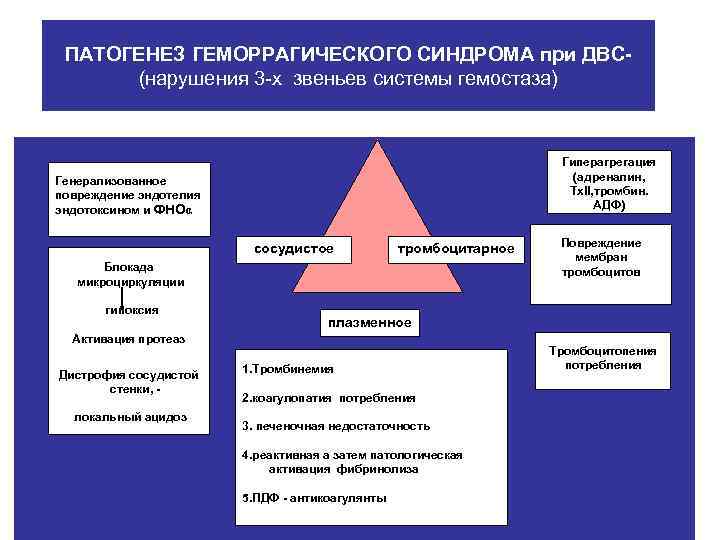 ПАТОГЕНЕЗ ГЕМОРРАГИЧЕСКОГО СИНДРОМА при ДВС- (нарушения 3 -х звеньев системы гемостаза) Генерализованное • Гиперагрегация (адреналин, повреждение эндотелия Тх. II, тромбин. эндотоксином и ФНОα АДФ) Повреждение сосудистое тромбоцитарное мембран Блокада тромбоцитов микроциркуляции гипоксия плазменное Активация протеаз Тромбоцитопения 1. Тромбинемия потребления Дистрофия сосудистой стенки, - 2. коагулопатия потребления локальный ацидоз 3. печеночная недостаточность 4. реактивная а затем патологическая активация фибринолиза 5. ПДФ - антикоагулянты
ПАТОГЕНЕЗ ГЕМОРРАГИЧЕСКОГО СИНДРОМА при ДВС- (нарушения 3 -х звеньев системы гемостаза) Генерализованное • Гиперагрегация (адреналин, повреждение эндотелия Тх. II, тромбин. эндотоксином и ФНОα АДФ) Повреждение сосудистое тромбоцитарное мембран Блокада тромбоцитов микроциркуляции гипоксия плазменное Активация протеаз Тромбоцитопения 1. Тромбинемия потребления Дистрофия сосудистой стенки, - 2. коагулопатия потребления локальный ацидоз 3. печеночная недостаточность 4. реактивная а затем патологическая активация фибринолиза 5. ПДФ - антикоагулянты
 Эффекты тромбина • Образование фибрина фибриногена и ф. II • Агрегация тромбоцитов количества тромбоцитов • Активация ф. V и ФVII уровня ФV и ФVII • Активация ФХIII • Активация системы протеина C и S (ПС/ПS) уровня ПС/ПS активация фибринолитическй системы
Эффекты тромбина • Образование фибрина фибриногена и ф. II • Агрегация тромбоцитов количества тромбоцитов • Активация ф. V и ФVII уровня ФV и ФVII • Активация ФХIII • Активация системы протеина C и S (ПС/ПS) уровня ПС/ПS активация фибринолитическй системы
 Эффекты плазмина • Деградация фибрина ПДФ • Деградация фибриногена • уровня ф. V и ф. VIII содержания • Протеолиз ФВ ФХII и ФХI содержания • Протеолиз ФХIII его уровня Изменения в ГП тромбоцитарной мб
Эффекты плазмина • Деградация фибрина ПДФ • Деградация фибриногена • уровня ф. V и ф. VIII содержания • Протеолиз ФВ ФХII и ФХI содержания • Протеолиз ФХIII его уровня Изменения в ГП тромбоцитарной мб
 Патогенез геморрагий при ДВС • 1. Блокада микроциркуляторного русла сгустками фибрина, агрегатами клеток крови и ПДФ • 2. дистрофия стенок капилляров • 3. сладж- феномен • 4. гипоксически- ишемическое повреждение мембран • 5. ацидоз • 6. тромбоцитопения потребления (нарушение трофики эндотелиоцитов и сосудисто- тромбоцитарного гемостаза • 7. потребление плазменных прокоагулянтов • 8. потребление антикоагулянтов (АТ III, prot. C, S).
Патогенез геморрагий при ДВС • 1. Блокада микроциркуляторного русла сгустками фибрина, агрегатами клеток крови и ПДФ • 2. дистрофия стенок капилляров • 3. сладж- феномен • 4. гипоксически- ишемическое повреждение мембран • 5. ацидоз • 6. тромбоцитопения потребления (нарушение трофики эндотелиоцитов и сосудисто- тромбоцитарного гемостаза • 7. потребление плазменных прокоагулянтов • 8. потребление антикоагулянтов (АТ III, prot. C, S).
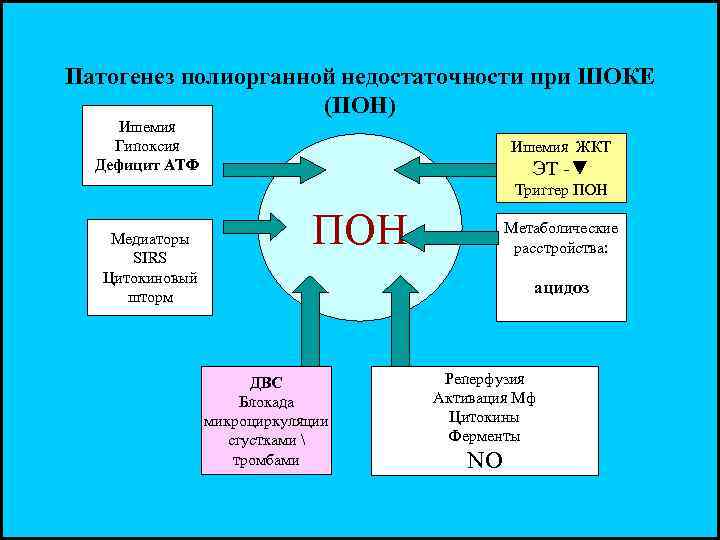 Патогенез полиорганной недостаточности при ШОКЕ (ПОН) Ишемия Гипоксия Ишемия ЖКТ Дефицит АТФ ЭТ -▼ Триггер ПОН Медиаторы SIRS ПОН Метаболические расстройства: Цитокиновый шторм ацидоз ДВС Реперфузия Блокада Активация Мф микроциркуляции Цитокины сгустками Ферменты тромбами NO
Патогенез полиорганной недостаточности при ШОКЕ (ПОН) Ишемия Гипоксия Ишемия ЖКТ Дефицит АТФ ЭТ -▼ Триггер ПОН Медиаторы SIRS ПОН Метаболические расстройства: Цитокиновый шторм ацидоз ДВС Реперфузия Блокада Активация Мф микроциркуляции Цитокины сгустками Ферменты тромбами NO
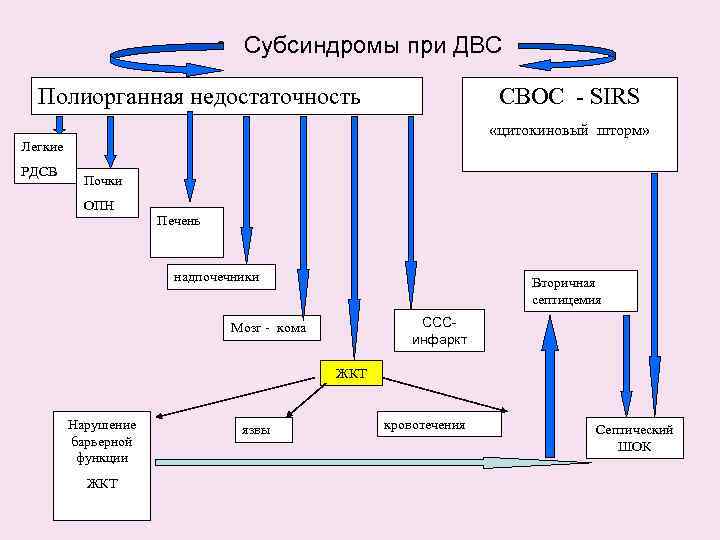 • Субсиндромы при ДВС Полиорганная недостаточность СВОС - SIRS «цитокиновый шторм» Легкие РДСВ Почки ОПН Печень надпочечники Вторичная септицемия Мозг - кома ССС- инфаркт ЖКТ Нарушение язвы кровотечения Септический барьерной ШОК функции ЖКТ
• Субсиндромы при ДВС Полиорганная недостаточность СВОС - SIRS «цитокиновый шторм» Легкие РДСВ Почки ОПН Печень надпочечники Вторичная септицемия Мозг - кома ССС- инфаркт ЖКТ Нарушение язвы кровотечения Септический барьерной ШОК функции ЖКТ
 Ведущие звенья патогенеза ДВС синдрома : 1) ” Протеолитический взрыв ” - чрезмерное образование тромбина и плазмина в крови вазоактивный эффект кининов, активация комплемента, «цитокиновый шторм» поступление клеточных протеаз патологический фибринолиз. 2) Системное поражение эндотелия вследствие ацидоза, эндотоксикоза, экзотоксикоза, гиперцитокинемии. 3) Гиперкоагуляция, связанная с активацией как внутреннего, так и внешнего путей коагуляции, при ведущей роли внешнего; 3) Блокада микроциркуляции на ранних стадиях ДВС за счет образования растворимых комплексов фибрин- фибриноген ( РФМК ) и развития фибриновых микротромбов и далее реологической окклюзии капилляров (повышение вязкости крови - сладж, сгустки). 5) Гипоксия и деструкция клеток с дисфункцией: ЦНС, почек, легких, печени, сердца -” полиорганная недостаточность ”. 6) Коагулопатия и тромбоцитопения потребления с истощением в крови уровней как прокоагулянтов (I II V VIII XIII f W ) так и естественных антикоагулянтов-ингибиторов активных сериновых протеаз (АТ III протеины C S и др. ). По мнению многих авторов, обеднение крови факторами свертывания, по крайней мере, во II стадии ДВС-синдрома, является скорее результатом удержания их в ретикулоэндотелии, чем потреблением при образовании внутрисосудистых тромбов. 7) Патологический фибринолиз со значительным повышением ПДФ деградацией фибриногена протеолизом V VIII XI XIII f W изменениями в гликопротеинах тромбоцитарной мембраны что нарушает как первичные так и вторичный гемостаз приводя к одновременному и последовательному развитию, как тромбозов так и склонности к кровотечению.
Ведущие звенья патогенеза ДВС синдрома : 1) ” Протеолитический взрыв ” - чрезмерное образование тромбина и плазмина в крови вазоактивный эффект кининов, активация комплемента, «цитокиновый шторм» поступление клеточных протеаз патологический фибринолиз. 2) Системное поражение эндотелия вследствие ацидоза, эндотоксикоза, экзотоксикоза, гиперцитокинемии. 3) Гиперкоагуляция, связанная с активацией как внутреннего, так и внешнего путей коагуляции, при ведущей роли внешнего; 3) Блокада микроциркуляции на ранних стадиях ДВС за счет образования растворимых комплексов фибрин- фибриноген ( РФМК ) и развития фибриновых микротромбов и далее реологической окклюзии капилляров (повышение вязкости крови - сладж, сгустки). 5) Гипоксия и деструкция клеток с дисфункцией: ЦНС, почек, легких, печени, сердца -” полиорганная недостаточность ”. 6) Коагулопатия и тромбоцитопения потребления с истощением в крови уровней как прокоагулянтов (I II V VIII XIII f W ) так и естественных антикоагулянтов-ингибиторов активных сериновых протеаз (АТ III протеины C S и др. ). По мнению многих авторов, обеднение крови факторами свертывания, по крайней мере, во II стадии ДВС-синдрома, является скорее результатом удержания их в ретикулоэндотелии, чем потреблением при образовании внутрисосудистых тромбов. 7) Патологический фибринолиз со значительным повышением ПДФ деградацией фибриногена протеолизом V VIII XI XIII f W изменениями в гликопротеинах тромбоцитарной мембраны что нарушает как первичные так и вторичный гемостаз приводя к одновременному и последовательному развитию, как тромбозов так и склонности к кровотечению.
 Лечение больных с ДВС-синдромом – искусство, основанное на сочетании знаний, умения наблюдать и замечать, анализировать и синтезировать, оперативно принимать решение и оценивать “обратную связь” – ответ больного на терапию.
Лечение больных с ДВС-синдромом – искусство, основанное на сочетании знаний, умения наблюдать и замечать, анализировать и синтезировать, оперативно принимать решение и оценивать “обратную связь” – ответ больного на терапию.
 ПРИНЦИПЫ И ТЕРАПИИ ДВС . 1. Ситуационная оценка: ШОК, сепсис, акушерская патология и т п – возможность ДВС 2. Этиотропная терапия (противошоковая, антибиотики при сепсисе и т д) 3. СЗП на любой стадии ДВС восстанавливает дефицит про- и антикоагулянтов. 4. Деблокада микроциркуляции. Низкомолекулярные гепарины (надропарин - фраксипарин) 5. Восполнение объема при шоках 6. Возмещение дефицита эритроцитов и тромбоцитов 7. . С 1 -ИН при сепсисе блокирует и комплемент и кинины и Х!!ф, предотвращая васкулит (особенно при менингококцемии) 8. Протеин S (особенно при септическом ДВС) 9. Борьба с ОПН, ДН, СН 10. Дезинтоксикационная терапия.
ПРИНЦИПЫ И ТЕРАПИИ ДВС . 1. Ситуационная оценка: ШОК, сепсис, акушерская патология и т п – возможность ДВС 2. Этиотропная терапия (противошоковая, антибиотики при сепсисе и т д) 3. СЗП на любой стадии ДВС восстанавливает дефицит про- и антикоагулянтов. 4. Деблокада микроциркуляции. Низкомолекулярные гепарины (надропарин - фраксипарин) 5. Восполнение объема при шоках 6. Возмещение дефицита эритроцитов и тромбоцитов 7. . С 1 -ИН при сепсисе блокирует и комплемент и кинины и Х!!ф, предотвращая васкулит (особенно при менингококцемии) 8. Протеин S (особенно при септическом ДВС) 9. Борьба с ОПН, ДН, СН 10. Дезинтоксикационная терапия.
 Стадии ДВС-синдрома 1 - гиперкоагуляция ( укорочение времени АЧТВ, ПТВ, положительные паракоагуляционные тесты, фрагментация эритроцитов в мазке, возможно снижение агрегационной функции тромбоцитов и активация фибринолиза). 2 - переходная (с нарастающей коагулопатией и тромбоцитопенией, характеризуется разнонаправленными сдвигами в общекоагуляционных тестах. Тромбоэластограмма – указывает гипокоагуляцию , а паракоагуляционные тесты – гиперкоагуляцю. ). 3 - гипокоагуляция ( удлинение времени всех общекоагуляционных тестов вплоть до несвертывания крови) , тромбоцитопения, анемия, дефицит фибриногена, АТ 111, протеинов С и S , патологически й фибринолиз. Кровотечения из мест инъекций. 4 – восстановительная (или при неблагоприятном течении фаза исходов и осложнений).
Стадии ДВС-синдрома 1 - гиперкоагуляция ( укорочение времени АЧТВ, ПТВ, положительные паракоагуляционные тесты, фрагментация эритроцитов в мазке, возможно снижение агрегационной функции тромбоцитов и активация фибринолиза). 2 - переходная (с нарастающей коагулопатией и тромбоцитопенией, характеризуется разнонаправленными сдвигами в общекоагуляционных тестах. Тромбоэластограмма – указывает гипокоагуляцию , а паракоагуляционные тесты – гиперкоагуляцю. ). 3 - гипокоагуляция ( удлинение времени всех общекоагуляционных тестов вплоть до несвертывания крови) , тромбоцитопения, анемия, дефицит фибриногена, АТ 111, протеинов С и S , патологически й фибринолиз. Кровотечения из мест инъекций. 4 – восстановительная (или при неблагоприятном течении фаза исходов и осложнений).
 Ведущие звенья патогенеза ДВС синдрома : 1) ”Протеолитический взрыв” - чрезмерное образование тромбина и плазмина в крови вазоактивный эффект кининов, активация комплемента, «цитокиновый шторм» поступление клеточных протеаз патологический фибринолиз. 2) Системное поражение эндотелия вследствие ацидоза, эндотоксикоза, экзотоксикоза, гиперцитокинемии. 3) Гиперкоагуляция , связанная с активацией как внутреннего, так и внешнего путей коагуляции, при ведущей роли внешнего; 3) Блокада микроциркуляции на ранних стадиях ДВС за счет образования растворимых комплексов фибрин-фибриноген и развития фибриновых микротромбов и далее реологической окклюзии капилляров (повышение вязкости крови - сладж, сгустки). 5) Гипоксия и деструкция клеток с дисфункцией: ЦНС, почек, легких, печени, сердца -”полиорганная недостаточность ”. 6) Коагулопатия и тромбоцитопения потребления с истощением в крови уровней как прокоагулянтов (I II V VIII XIII f W) так и естественных антикоагулянтов-ингибиторов активных сериновых протеаз (АТ III протеины C S и др. ). По мнению многих авторов, обеднение крови факторами свертывания, по крайней мере, во II стадии ДВС-синдрома, является скорее результатом удержания их в ретикулоэндотелии, чем потреблением при образовании внутрисосудистых тромбов. 7) Патологический фибринолиз со значительным повышением ПДФ деградацией фибриногена протеолизом V VIII XI XIII f W изменениями в гликопротеинах тромбоцитарной мембраны что нарушает как первичные так и вторичный гемостаз приводя к одновременному и последовательному развитию, как тромбозов так и склонности к кровотечению.
Ведущие звенья патогенеза ДВС синдрома : 1) ”Протеолитический взрыв” - чрезмерное образование тромбина и плазмина в крови вазоактивный эффект кининов, активация комплемента, «цитокиновый шторм» поступление клеточных протеаз патологический фибринолиз. 2) Системное поражение эндотелия вследствие ацидоза, эндотоксикоза, экзотоксикоза, гиперцитокинемии. 3) Гиперкоагуляция , связанная с активацией как внутреннего, так и внешнего путей коагуляции, при ведущей роли внешнего; 3) Блокада микроциркуляции на ранних стадиях ДВС за счет образования растворимых комплексов фибрин-фибриноген и развития фибриновых микротромбов и далее реологической окклюзии капилляров (повышение вязкости крови - сладж, сгустки). 5) Гипоксия и деструкция клеток с дисфункцией: ЦНС, почек, легких, печени, сердца -”полиорганная недостаточность ”. 6) Коагулопатия и тромбоцитопения потребления с истощением в крови уровней как прокоагулянтов (I II V VIII XIII f W) так и естественных антикоагулянтов-ингибиторов активных сериновых протеаз (АТ III протеины C S и др. ). По мнению многих авторов, обеднение крови факторами свертывания, по крайней мере, во II стадии ДВС-синдрома, является скорее результатом удержания их в ретикулоэндотелии, чем потреблением при образовании внутрисосудистых тромбов. 7) Патологический фибринолиз со значительным повышением ПДФ деградацией фибриногена протеолизом V VIII XI XIII f W изменениями в гликопротеинах тромбоцитарной мембраны что нарушает как первичные так и вторичный гемостаз приводя к одновременному и последовательному развитию, как тромбозов так и склонности к кровотечению.
 Патогенез гемостазиологических расстройств при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей роли ВНЕШНЕГО системное поражение эндотелия ”Протеолитический взрыв”- вследствие активации 4 -х плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ геморрагический синдром калликреин-кининовой АД ¸ повышение сосудистой проницаемости Комплемента стимуляция всех звеньев гемостаза поступления клеточных протеаз Коагулопатия и эндотоксинемия тромбоцитопения Эндотоксикоз потребления с Цитокиновый «шторм» истощением про- и антикоагулянтов (I II V VIII XIII Патологический АТ III протеинов C S фибринолиз Увеличение. ПДФ Тромбо - геморрагический синдром
Патогенез гемостазиологических расстройств при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей роли ВНЕШНЕГО системное поражение эндотелия ”Протеолитический взрыв”- вследствие активации 4 -х плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ геморрагический синдром калликреин-кининовой АД ¸ повышение сосудистой проницаемости Комплемента стимуляция всех звеньев гемостаза поступления клеточных протеаз Коагулопатия и эндотоксинемия тромбоцитопения Эндотоксикоз потребления с Цитокиновый «шторм» истощением про- и антикоагулянтов (I II V VIII XIII Патологический АТ III протеинов C S фибринолиз Увеличение. ПДФ Тромбо - геморрагический синдром
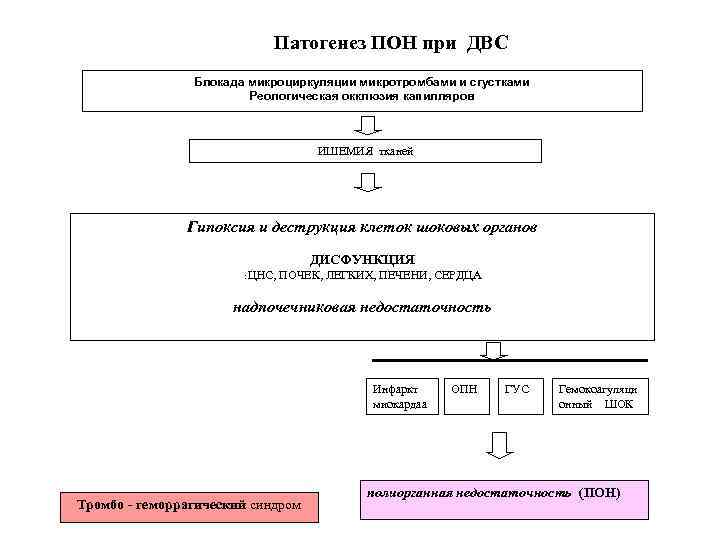 Патогенез ПОН при ДВС Блокада микроциркуляции микротромбами и сгустками Реологическая окклюзия капилляров ИШЕМИЯ тканей Гипоксия и деструкция клеток шоковых органов ДИСФУНКЦИЯ : ЦНС, ПОЧЕК, ЛЕГКИХ, ПЕЧЕНИ, СЕРДЦА надпочечниковая недостаточность Инфаркт ОПН ГУС Гемокоагуляци миокардаа онный ШОК полиорганная недостаточность (ПОН) Тромбо - геморрагический синдром
Патогенез ПОН при ДВС Блокада микроциркуляции микротромбами и сгустками Реологическая окклюзия капилляров ИШЕМИЯ тканей Гипоксия и деструкция клеток шоковых органов ДИСФУНКЦИЯ : ЦНС, ПОЧЕК, ЛЕГКИХ, ПЕЧЕНИ, СЕРДЦА надпочечниковая недостаточность Инфаркт ОПН ГУС Гемокоагуляци миокардаа онный ШОК полиорганная недостаточность (ПОН) Тромбо - геморрагический синдром
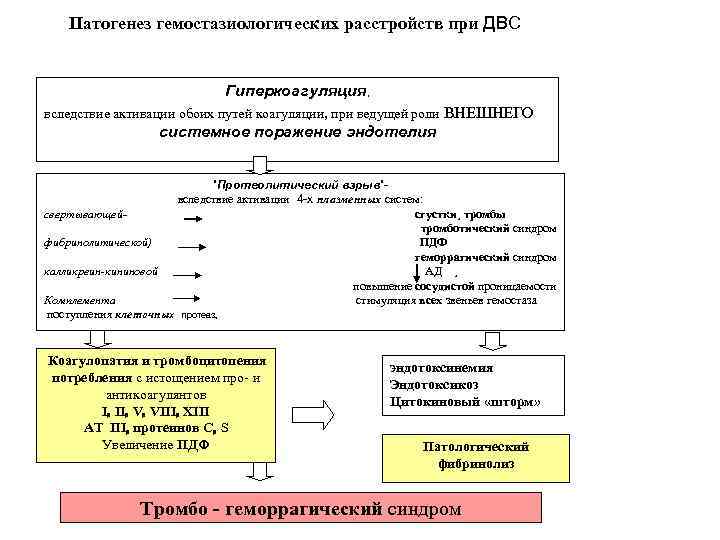 Патогенез гемостазиологических расстройств при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей роли ВНЕШНЕГО системное поражение эндотелия ”Протеолитический взрыв”- вследствие активации 4 -х плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ геморрагический синдром калликреин-кининовой АД ¸ повышение сосудистой проницаемости Комплемента стимуляция всех звеньев гемостаза поступления клеточных протеаз Коагулопатия и тромбоцитопения эндотоксинемия потребления с истощением про- и Эндотоксикоз антикоагулянтов Цитокиновый «шторм» I II V VIII XIII АТ III протеинов C S Увеличение ПДФ Патологический фибринолиз Тромбо - геморрагический синдром
Патогенез гемостазиологических расстройств при ДВС Гиперкоагуляция, вследствие активации обоих путей коагуляции, при ведущей роли ВНЕШНЕГО системное поражение эндотелия ”Протеолитический взрыв”- вследствие активации 4 -х плазменных систем: свертывающей- сгустки¸ тромбы тромботический синдром фибринолитической) ПДФ геморрагический синдром калликреин-кининовой АД ¸ повышение сосудистой проницаемости Комплемента стимуляция всех звеньев гемостаза поступления клеточных протеаз Коагулопатия и тромбоцитопения эндотоксинемия потребления с истощением про- и Эндотоксикоз антикоагулянтов Цитокиновый «шторм» I II V VIII XIII АТ III протеинов C S Увеличение ПДФ Патологический фибринолиз Тромбо - геморрагический синдром
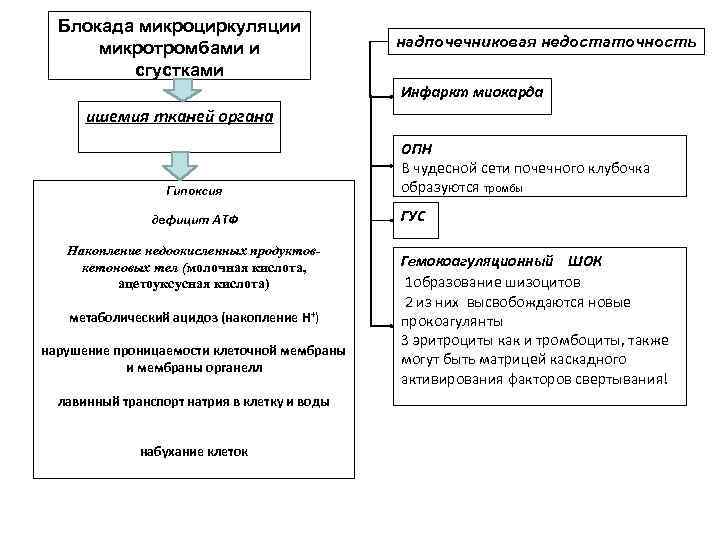 Блокада микроциркуляции микротромбами и надпочечниковая недостаточность сгустками Инфаркт миокарда ишемия тканей органа ОПН В чудесной сети почечного клубочка Гипоксия образуются тромбы дефицит АТФ ГУС Накопление недоокисленных продуктов- кетоновых тел (молочная кислота, Гемокоагуляционный ШОК ацетоуксусная кислота) 1 образование шизоцитов 2 из них высвобождаются новые метаболический ацидоз (накопление Н+) прокоагулянты 3 эритроциты как и тромбоциты, также нарушение проницаемости клеточной мембраны и мембраны органелл могут быть матрицей каскадного активирования факторов свертывания! лавинный транспорт натрия в клетку и воды набухание клеток
Блокада микроциркуляции микротромбами и надпочечниковая недостаточность сгустками Инфаркт миокарда ишемия тканей органа ОПН В чудесной сети почечного клубочка Гипоксия образуются тромбы дефицит АТФ ГУС Накопление недоокисленных продуктов- кетоновых тел (молочная кислота, Гемокоагуляционный ШОК ацетоуксусная кислота) 1 образование шизоцитов 2 из них высвобождаются новые метаболический ацидоз (накопление Н+) прокоагулянты 3 эритроциты как и тромбоциты, также нарушение проницаемости клеточной мембраны и мембраны органелл могут быть матрицей каскадного активирования факторов свертывания! лавинный транспорт натрия в клетку и воды набухание клеток
 Патогенез полиорганной недостаточности при ШОКЕ (ПОН) Ишеимя Ишемия ЖКТ Гипоксия ЭТ -▼ Дефицит АТФ Триггер ПОН Медиаторы SIRS ПОН Метаболические расстройства: ДВС ацидоз Блокада микроциркуляции нарушение сгустками утилизации тромбами глюкозы и Реперфузия жирных кислот Активация Мф Цитокины дефицит АТФ Ферменты ШОКОВАЯ NO КЛЕТКА
Патогенез полиорганной недостаточности при ШОКЕ (ПОН) Ишеимя Ишемия ЖКТ Гипоксия ЭТ -▼ Дефицит АТФ Триггер ПОН Медиаторы SIRS ПОН Метаболические расстройства: ДВС ацидоз Блокада микроциркуляции нарушение сгустками утилизации тромбами глюкозы и Реперфузия жирных кислот Активация Мф Цитокины дефицит АТФ Ферменты ШОКОВАЯ NO КЛЕТКА
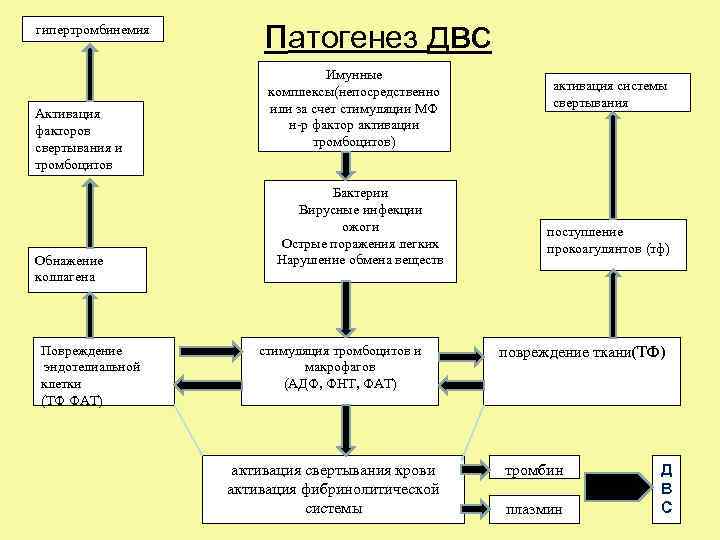 гипертромбинемия патогенез двс Имунные комплексы(непосредственно активация системы или за счет стимуляции МФ свертывания Активация факторов н-р фактор активации свертывания и тромбоцитов) тромбоцитов Бактерии Вирусные инфекции ожоги поступление Острые поражения легких прокоагулянтов (тф) Обнажение Нарушение обмена веществ коллагена Повреждение стимуляция тромбоцитов и повреждение ткани(ТФ) эндотелиальной макрофагов клетки (АДФ, ФНТ, ФАТ) (ТФ ФАТ) активация свертывания крови тромбин Д активация фибринолитической В системы плазмин С
гипертромбинемия патогенез двс Имунные комплексы(непосредственно активация системы или за счет стимуляции МФ свертывания Активация факторов н-р фактор активации свертывания и тромбоцитов) тромбоцитов Бактерии Вирусные инфекции ожоги поступление Острые поражения легких прокоагулянтов (тф) Обнажение Нарушение обмена веществ коллагена Повреждение стимуляция тромбоцитов и повреждение ткани(ТФ) эндотелиальной макрофагов клетки (АДФ, ФНТ, ФАТ) (ТФ ФАТ) активация свертывания крови тромбин Д активация фибринолитической В системы плазмин С
present5.com
Бактериальный шок и ДВС-синдром входят в тему курса общей патологической анатомии «Расстройства кровообращения» и частной патологической анатомии «Сепсис, бактериальный шок и ДВС-синдром».
Общее время занятия: 3 часа для студентов лечебного, педиатрического, медико-профилактического факультетов и факультета иностранных учащихся; 1,5 часа для студентов стомфака.
Мотивационная характеристика темы: бактериальный шок и ДВС-синдром занимают особое место в патологии человека. Согласно статистическим данным количество случаев этих патологических процессов значительно увеличилось. Это требует от врачей доскональных знаний об их этиологии, патогенезе и клинико-морфологической характеристике, так как подобные вопросы в должной мере не отражены в существующих учебниках патологической анатомии.
Цель занятия: изучить особенности этиологии и патогенеза, клинико-морфологические признаки бактериального шока и ДВС-синдрома.
Задачи занятия: ознакомиться с особенностями этиологии и патогенеза бактериального шока и ДВС-синдрома, научиться патоморфологически диагностировать эти патологические процессы.
Требования к исходному уровню знаний: для полного усвоения материала студенту необходимо повторить из курса биохимии систему гемостаза.
Контрольные вопросы из смежных дисциплин:
1. Стадии гемостаза.
2. Основные проявления сосудисто-тромбоцитарного гемостаза.
3. Стадии и основные проявления коагуляционного гемостаза.
4. Противосвертывающая система.
Контрольные вопросы по теме занятия:
1. Определение, особенности этиологии и патогенеза бактериального
шока.
2. «Факторы прорыва» при бактериальном шоке.
3. Патоморфологическая характеристика бактериального шока.
4. Определение, особенности этиологии и патогенеза ДВС-синдрома.
5. Патоморфологические проявления ДВС-синдрома.
6. Морфологические особенности ДВС-синдрома при гнойно-септических заболеваниях.
Бактериальный шок (БШ) - (сип.: бактериемический, бактериотоксический, эндотоксический, септический шок): патологический процесс, осложняющий многие инфекционные заболевания и хирургические инфекции, характеризующийся быстро развивающимися выраженными расстройствами центральной и периферической гемодинамики в ответ на массивную инвазию бактериальных и тканевых токсинов, а также биологически активных аминов.
По частоте БШ следует за травматическим, геморрагическим и кардиогенным шоками, но по летальности он находится на первом месте.
Клинические проявления БШ не зависят от этиологии: внезапное падение артериального давления, снижение температуры тела, тахикардия, холодный пот, анурия, адинамия, вялость.
Этот патологический процесс могут вызывать бактерии, реже грибы, риккетсии и вирусы. В подавляющем большинстве случаев БШ обусловлен грамотрицательной аэробной бактериальной флорой: Esherichia coli, Clebsiella из рода Proteus, Pseudomonas aeruginosa, aerogenes. Вероятнее всего, токсическим эффектом обладают не столько бактериальные токсины, сколько их смесь с протеиногенными аминами, образующимися в первичном очаге поражения. Поэтому клинико-анатомическая картина, аналогичная БШ, может развиваться и при безмикробном протеолизе в первичном очаге, например при ретроплацентарной гематоме, синдроме «мертвого плода», а также в эксперименте с инъекцией гистамина и других протеиногенных аминов.
Для развития БШ необходимо по крайней мере два обязательных фактора:
1. Первичный очаг (входные ворота), в качестве которого чаще всего выступают: мочевые пути (пиелонефрит), желчевыводящие пути (холангит и холангиолит), брюшина (перитонит), кишечник (энтероколит), бронхи и легкие (пневмонии и абсцессы легких), кожа и подкожная жировая клетчатка (флегмона и ожоги), гениталии (послеабортный эндометрит, хориоамнионит и др.), сосуды (катетеризационный тромбофлебит) и др.
2. «Факторы прорыва» - условия для резорбции токсических продуктов из первичного очага:
а) повреждение биологических барьеров, локализующих инфекцию в первичном очаге: неправильная вторичная обработка гнойной раны, хирургическое вмешательство, инструментальное исследование, обработка раны протеолитическими ферментами и т.п.;
б) снижение резистентности организма больного;
в) токсическое повреждение антибактериальными препаратами стенки кишечника, увеличивающее ее проницаемость для бактерий;
г) высокая вирулентность микроорганизмов или их массивный лизис с быстро наступающим высвобождением большого количества эндотоксинов при использовании высокоэффективных антибиотиков и др.
Патогенез бактериального шока складывается из следующих процессов, быстро развивающихся в ответ на массивную инвазию бактериальных и тканевых токсинов, а также биологически активных аминов из первичного очага: повреждение эндотелия преимущественно микроциркуляторного русла (МЦР), шоковые расстройства гемодинамики, ДВС-синдром, альтеративные изменения органов. Шоковые расстройства гемодинамики проявляются в виде децентрализации кровотока с секвестрацией крови в МЦР, шунтировании кровотока. ДВС-синдром имеет острейшее течение с короткой фазой гиперкоагуляции, быстро сменяемой гипокоагуляцией, вследствие чего доминируют проявления геморрагического синдрома. Альтеративные (дистрофические и некротические) изменения носят полиорганный характер и обусловлены шоковыми расстройствами гемодинамики и ДВС-синдромом.
В патогенезе БШ большое значение имеют также иммунные факторы, поступающие в кровоток медиаторы воспаления (гистамин, серотонин и др.), катехоламины, активация калликреин-кининовой системы и др.
studfiles.net
 ГлавнаяСтатьиОпросыКонтактыРегистрацияВход
ГлавнаяСтатьиОпросыКонтактыРегистрацияВход Поиск:
 Расшифровка анализов
Расшифровка анализов Разделы
Разделы Заболевания по алфавиту
Заболевания по алфавиту Врачи
Врачи Симптомы и признаки
Симптомы и признаки
meddex.ru